G. Johansson, A. Lindberg, K. Romberg, L. Nordstrom, A. Roquet, Швеция, F. Gerken, Германия
Хроническое обструктивное заболевание легких (ХОЗЛ) – широко распространенная в популяции медленно прогрессирующая патология. Как правило, диагноз ХОЗЛ устанавливают уже при появлении клинических симптомов, после длительного латентного течения.
Эпидемиологическая программа исследований, охватившая северные регионы Швеции, выявила распространенность ХОЗЛ на уровне 14,3%, при этом большая часть пациентов (57%) имели легкое заболевание согласно критериям Глобальной инициативы по борьбе с ХОЗЛ (GOLD), а именно отношение объема форсированного выдоха за 1 с после назначения бронхолитика и форсированной жизненной емкости легких (ОФВ1/ФЖЕЛ) <70% и ОФВ1≥80% от должного [2, 3]. Несмотря на то что 70% пациентов имели симптомы, ранее диагноз ХОЗЛ был установлен только у 5% [2]. Еще большую обеспокоенность вызывает тот факт, что, хотя у всех пациентов с тяжелым и очень тяжелым ХОЗЛ (6% всех случаев) были клинические симптомы, только 50% из них имели диагноз, установленный лечащим терапевтом.
Бронхолитики, принимаемые по требованию или регулярно, обеспечивают больным ХОЗЛ симптоматическую помощь. Нерешенным остается вопрос об оптимальном времени, когда следует начинать такую поддерживающую терапию. Стандартным маркером прогрессии заболевания считается снижение ОФВ1, однако с течением времени ухудшаются и другие показатели, такие как одышка, физическая активность, частота обострений и качество жизни, связанное со здоровьем (КЖСЗ) [4]. Поэтому очевидно, что пациент, которому установили диагноз ХОЗЛ, должен получить адекватное лечение, в том числе профилактическое, как можно раньше.
Тиотропий (Спирива®, Boehringer Ingelheim GmbH, Германия) – холинолитик, назначаемый 1 раз в сутки, действующий путем пролонгированной блокады мускариновых М3-рецепторов. В клинических исследованиях тиотропий улучшал легочную функцию и субъективные показатели эффективности лечения, такие как качество жизни [5-9]. Ретроспективный анализ более ранних исследований показал, что тиотропий может оказывать благоприятные эффекты и у пациентов с ХОЗЛ легкой степени (согласно критериям GOLD) [10]. Тем не менее проспективные исследования, в которых бы целенаправленно изучали эффективность препарата при ХОЗЛ легкой степени, до настоящего времени не проводились.
В Швеции в 2003 г. ХОЗЛ легкой степени определялось как ОФВ1/ФЖЕЛ <70% и ОФВ1 ≥60% от должного (критерии Шведского общества респираторной медицины) [11]. Это определение соответствовало критериям Британского торакального общества (BTS, 1997) для ХОЗЛ легкой степени (ОФВ1 60-80% от должного) [12] и было сравнимым с указанной в руководстве Американского торакального общества (ATS, 1995) I стадией ХОЗЛ (ОФВ1 ≥50% от должного) [13]. На сегодняшний день в Швеции ХОЗЛ легкой степени тяжести определяется как ОФВ1/ФЖЕЛ <70% и ОФВ1 50-79% от должного [14]. По состоянию на 2003 г. шведские руководства не содержали стандартных терапевтических рекомендаций для пациентов с ХОЗЛ легкой степени [11].
Целью настоящего исследования было оценить эффекты тиотропия, назначаемого по 18 мкг 1 раз в день, на легочную функцию, клинические симптомы и КЖСЗ у пациентов с ХОЗЛ легкой степени согласно определению шведского руководства 2003 г., что соответствует ХОЗЛ легкой и средней степени тяжести по критериям GOLD.
Материалы и методы
Пациенты
В исследовании приняли участие амбулаторные пациенты, соответствующие следующим критериям включения: возраст 40 лет и старше; диагноз ХОЗЛ легкой степени согласно шведскому руководству за 2003 г. (ОФВ1/ФЖЕЛ <70% и ОФВ1 ≥60% от должного); анамнез курения ≥10 пачко-лет; одышка по шкале Медицинского исследовательского совета (MRC) 2 балла и выше.
Критерии исключения: бронхиальная астма, аллергический ринит, атопия в анамнезе; эозинофилы крови ≥600/мм3; недавно перенесенная инфекция нижних дыхательных путей или ее обострение (в предшествующие 6 нед); недавно перенесенный инфаркт миокарда (в предшествующие 6 мес); нестабильная сердечная аритмия; регулярное использование оксигенотерапии; использование кортикостероидов внутрь или ингаляционно (за последние 3 мес); наличие других (кроме ХОЗЛ) значимых заболеваний.
Дизайн исследования
Рандомизированное двойное слепое многоцентровое исследование в параллельных группах продолжалось 12 нед. Протокол исследования был утвержден Наблюдательным комитетом. Все участники предоставили письменное информированное согласие.
Первичной конечной точкой было изменение площади под кривой ОФВ1 за период от момента перед назначением препарата до 2 ч после назначения (AUC0-2 ч) через 12 нед лечения. Вторичными конечными точками были изменение ОФВ1 и ФЖЕЛ, использование скоропомощных препаратов и частота неблагоприятных событий (НС). Одышку и КЖСЗ оценивали при помощи опросников.
Методы исследования
После скринингового визита за пациентами наблюдали в течение 2 нед. После дополнительного обследования в 1-й день исследования пациентов рандомизировали 1:1 для получения тиотропия 18 мкг или плацебо 1 раз/сут утром на протяжении 12 нед, которые пациенты вводили с помощью доставочного устройства HandiHaler® (Boehringer Ingelheim). Следующие обследования проводили в 15-й (через 2 нед) и 86-й (через 12 нед) день исследования. Референтным значением AUC0-2 ч был показатель, который получали в 1-й день до назначения первой дозы. В качестве скоропомощного препарата для облегчения острых симптомов пациенты могли использовать сальбутамол по требованию (через дозатор-ингалятор), с 8-часовым «отмывочным» периодом до проведения спирометрии. Использование короткодействующих холинолитиков, β2-агонистов (кроме сальбутамола), пероральных и ингаляционных кортикостероидов и теофиллина не разрешалось. Однако для лечения обострения ХОЗЛ лечащий врач мог назначать антибиотики и кортикостероиды внутрь (на период не более 2 нед) и теофиллин (не более 7 дней). В случае обострения ХОЗЛ спирометрию откладывали на 1-2 нед после завершения его лечения.
Спирометрию проводили при скрининге и в 1, 15-й и 85-й день исследования. ОФВ1 и ФЖЕЛ регистрировали за 10 мин до и через 0,5; 1 и 2 ч после приема препарата. Изменения ОФВ1 и ФЖЕЛ под действием лечения определяли перед приемом препарата в 15-й и 85-й день. Все спирометрические исследования выполняли трехкратно, для последующего анализа использовали самые высокие значения. Использованное оборудование и методы соответствовали стандартам ATS (1994) и Европейского респираторного общества (ERS, 1993) [15, 16].
Опросники, позволяющие оценить одышку и КЖСЗ, пациенты заполняли в начале и в конце исследования. Одышку оценивали с помощью базисного индекса одышки BDI [17] и шкалы одышки MRC [18]. Индекс BDI состоит из трех подшкал (функциональное нарушение, степень выполнения задания и степень усилия для выполнения задания), по каждой из которых ставится оценка в баллах от 0 (очень тяжелое нарушение) до 4 (нарушения нет). Сумма баллов определяет общую оценку BDI (от 0 до 12). Ощущаемую выраженность одышки пациенты оценивали также по шкале MRC в баллах от 0 (нет одышки) до 5 (одышка не позволяет покинуть дом, или одышка при одевании/раздевании).
Качество жизни, связанное со здоровьем, оценивали с помощью Европейского опросника качества жизни EQ-5D [19, 20], который включает визуальную аналоговую шкалу (ВАШ) EQ-5D и индекс EQ-5D. ВАШ – рейтинговая шкала от 0 до 10 см, которые пациент представляет как 0-100% (0% – смерть/наихудшее состояние здоровья; 100% – наилучшее состояние здоровья). Индекс EQ-5D – опросник, состоящий из 5 категорий (способность передвигаться, самопомощь, повседневная активность, боль/дискомфорт и депрессия/тревога). Для каждой категории пациент выбирает одно из трех описательных состояний здоровья, после чего подсчитывается число/процент пациентов, выбравших каждое состояние.
Ежедневно пациенты отмечали количество использованных доз скоропомощного препарата. Также регистрировались неблагоприятные события, в том числе обострения ХОЗЛ.
Результаты
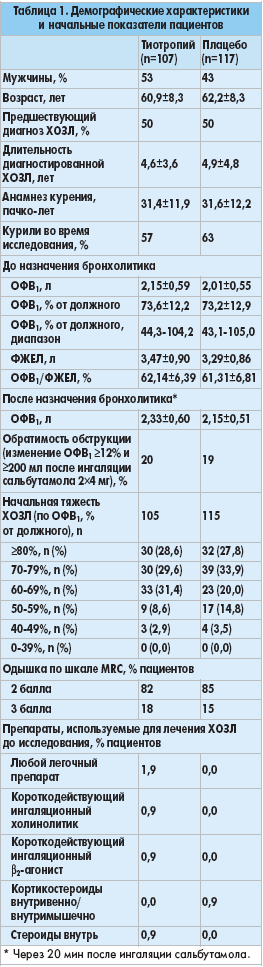
224 пациента рандомизировали для получения тиотропия (n=107) или плацебо (n=117). Исследование проводили с марта 2004 по июль 2005 года в 27 клинических центрах Швеции. Группы лечения были сравнимы по начальным значениям ОФВ1 (абсолютным и % от должного; табл. 1). Значимую обратимость обструкции (обратимость >12% и >200 мл) имели 20 и 19% пациентов в группах тиотрипия и плацебо соответственно. Все пациенты имели одышку по шкале MRC ≥2. Во всей популяции исследования I, II, III и IV стадии ХОЗЛ по определению GOLD имели соответственно 62 (28,2%), 151 (68,6%), 7 (3,2%) и 0 (0,0%) пациентов.
Спирометрия
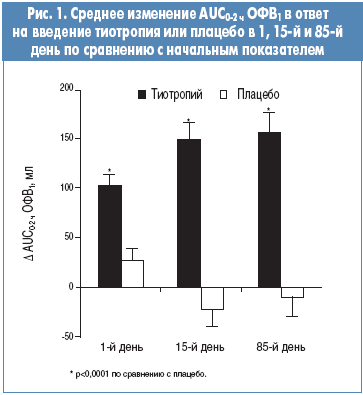
На 85-й день исследования AUC0-2 ч ОФВ1 (первичная конечная точка) в группе тиотропия улучшилась на 157±19 мл, в группе плацебо – ухудшилась на 9±18 мл по сравнению с начальным показателем (различие между группами 166±26 мл; р<0,0001; рис. 1). Значительное увеличение AUC0-2 ч ОФВ1 как ответ на препарат в группе тиотропия по сравнению с плацебо также наблюдалось в 1-й день (на 74±15 мл; р<0,0001) и 15-й день (на 172±22 мл, р<0,0001; рис. 1).
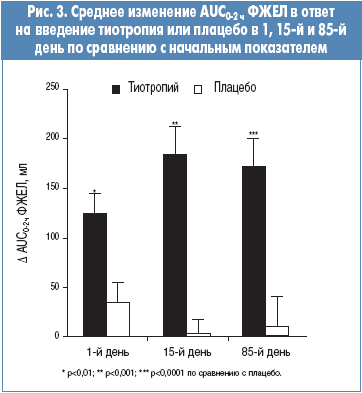
По сравнению с плацебо назначение тиотропия сопровождалось значительным расширением бронхов (увеличением ОФВ1) в пределах 30 мин после первой ингаляции – различие по сравнению с показателем до назначения в 1-й день между группами составило 35±18 мл (p<0,05). На рисунке 2 показано, что изменения ОФВ1 по сравнению с начальными были значительно лучше в группе тиотропия во всех временных точках и во все дни спирометрии (р<0,05 для всех сравнений с плацебо). Через 2 нед лечения показатель ОФВ1 улучшился на 109±20 мл по сравнению с плацебо (р<0,0001). В конце исследования показатель ОФВ1 у пациентов, получавших тиотропий, увеличился на 74±23 мл, а в группе плацебо, наоборот, снизился на 45±22 мл по сравнению с начальным показателем (различие между группами 118±31 мл, р<0,001). Кроме того, в группе тиотропия наблюдалось значительное улучшение AUC0-2 ч ОФВ1 и ОФВ1, % от должного (р<0,01 для всех временных точек).
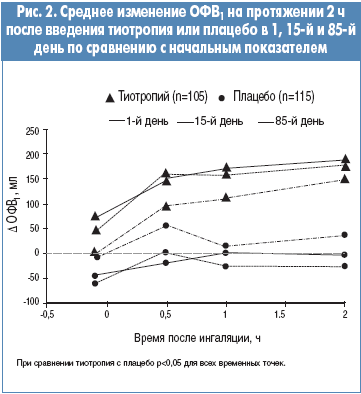
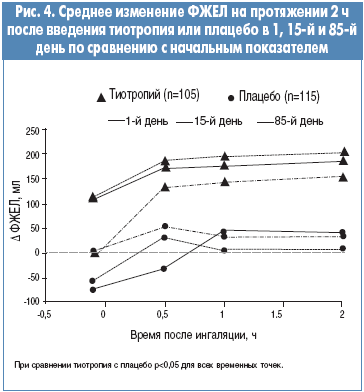
Для ФЖЕЛ получены примерно такие же результаты, как и для ОФВ1. Так, по сравнению с больными, получавшими плацебо, у пациентов группы тиотропия значительно улучшился показатель AUC0-2 ч ФЖЕЛ в 1-й день (на 89±27 мл, p<0,01), 15-й день (на 182±37 мл, p<0,0001) и 85-й день исследования (на 160±43 мл, p<0,001). Эти данные представлены на рисунке 3.
На рисунке 4 отображено статистически значимое улучшение ФЖЕЛ в группе тиотропия, наблюдаемое в 15-й (178±36 мл, p<0,0001) и 85-й день (187±50 мл, p<0,001).
Использование скоропомощных препаратов
Использование сальбутамола по требованию до рандомизации было низким (в группе тиотропия 0,71±0,05 доз/день; в группе плацебо 0,76±0,05 доз/день) и на протяжении исследования снижалось (на 12-й нед 0,23±0,05 и 0,29±0,05 доз/день соответственно). Пациенты, получавшие тиотропий, достоверно реже прибегали к ингаляции сальбутамола на протяжении первых 5 нед исследования, а также на 9-й нед (различие по сравнению с плацебо от 0,17 до 0,23 доз/день, р<0,05).
Одышка и качество жизни
Пациенты с ХОЗЛ легкой степени обеих групп испытывали лишь незначительную одышку, связанную с физической нагрузкой, а КЖСЗ было нарушено умеренно в начале и в конце исследования. Значимых различий между группами тиотропия и плацебо по общей оценке BDI по завершению исследования не было (8,57±0,11 vs. 8,45±0,11). Также в конце исследования в обеих группах было сравнимое число пациентов с улучшением, ухудшением или отсутствием изменений по шкале MRC; показатель ВАШ EQ-5D был одинаковым; в отношении общей оценки EQ-5D различий не было (тиотропий 0,83±0,01; плацебо 0,85±0,01).
Анализ подшкал EQ-5D показал, что большинство пациентов обеих групп (тиотропий vs. плацебо) не имели проблем с самопомощью (99,0 vs. 99,1%), ходьбой (82,9 vs. 87,0%) и выполнением повседневных задач (89,5 vs. 88,7%). В то же время в группе тиотропия по сравнению с группой плацебо было меньше пациентов, испытывающих боль/дискомфорт (47,6 vs. 49,6%) и умеренно выраженную тревогу или депрессию (25,7 vs. 31,3%).
Неблагоприятные события
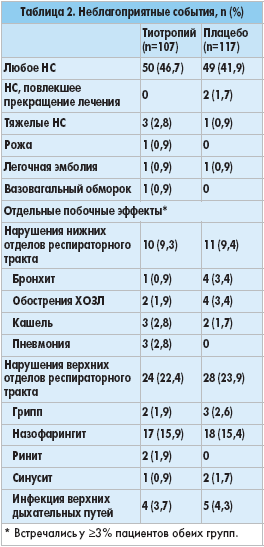
НС наблюдались с одинаковой частотой в обеих группах (табл. 2). Несмотря на то что у 2,8% пациентов группы тиотропия и у 0,9% группы плацебо были тяжелые НС, ни одно из них не было связано с лечением. В группе плацебо из-за НС прервали лечение два пациента (1,7%); среди получавших тиотропий таких случаев не было. Обострения ХОЗЛ развились у 2 пациентов (1,9%) на фоне лечения тиотропием и у 4 больных (3,4%) группы плацебо.
Обсуждение
Международное руководство GOLD рекомендует использовать длительно действующие холинолитики (тиотропий) в качестве поддерживающей терапии у пациентов со среднетяжелой, тяжелой и очень тяжелой степенью ХОЗЛ [3]. В настоящем исследовании изучали эффекты 12-недельного лечения тиотропием 18 мкг 1 раз в день на легочную функцию пациентов с ХОЗЛ легкой степени по определению шведского руководства за 2003 г., что соответствует легкой и средней степени тяжести ХОЗЛ по критериям GOLD [3, 11]. Начальный показатель ОФВ1 был сравнимым в обеих группах. У половины пациентов до начала исследования диагноз ХОЗЛ установлен не был, и менее 2% больных получали какое-либо лечение. По завершению исследования у пациентов, получавших тиотропий, значительно улучшилась легочная функция по сравнению как с начальными показателями, так и с плацебо. Это улучшение становилось очевидным уже через 30 мин после ингаляции и сохранялось 24 ч (до следующей дозы) и на протяжении всего периода исследования.
Пациенты, принявшие участие в настоящем исследовании, имели ХОЗЛ легкой и средней степени тяжести по критериям GOLD [3]. Нижняя граница легкого ХОЗЛ в шведском руководстве за 2003 г. находится в пределах ХОЗЛ средней степени тяжести по GOLD (ОФВ1 ≥50-80% от должного), в то время как при легком течении ХОЗЛ (GOLD) ОФВ1 должно быть 80% и выше [3, 11].
В современном шведском руководстве по ведению пациентов с ХОЗЛ сохранилась классификация тяжести 2003 г. (ХОЗЛ легкой степени: ОФВ1 50-79% от должного) [14], что соответствует средней степени тяжести по GOLD. Таким образом, если использовать классификацию GOLD, 28,2%, 68,8 и 3,2% пациентов имели соответственно ХОЗЛ легкой, средней и тяжелой степени. Распределение пациентов по группам тяжести в данном исследовании резко отличается от такого в других исследованиях с тиотропием. Метаанализ начальных характеристик пациентов – участников 24 предыдущих исследований с этим препаратом – показал, что лишь 0,2% больных ХОЗЛ имели стадию I по GOLD по сравнению с 26,9; 49,0 и 23,9% пациентов со средней тяжести, тяжелым и очень тяжелым ХОЗЛ. Уникальная особенность настоящего исследования состоит в том, что оно было специально спланировано для оценки эффективности тиотропия у пациентов с ХОЗЛ легкой степени, у которых заболевание в большинстве случаев на этой стадии не выявляется.
Полученные результаты подтверждают данные ретроспективных исследований о том, что тиотропий проявляет высокую эффективность у пациентов с начальными стадиями ХОЗЛ. У 1639 пациентов с ХОЗЛ различной тяжести 12-недельное лечение тиотропием привело к значительному улучшению показателя ОФВ1 (как до, так и через 2 ч после назначения препарата), при этом наиболее выраженные положительные изменения наблюдались у 531 пациента с легким заболеванием (ОФВ1 ≥50-70% по критериям ATS) [21]. Ретроспективный анализ двух однолетних исследований пациентов с ХОЗЛ, ранее не получавших поддерживающей терапии, показал, что в подгруппе из 20 больных с ХОЗЛ легкой степени тяжести (GOLD), которые принимали тиотропий, минимальные, максимальные и средние значения ОФВ1 и ФЖЕЛ значительно улучшились по сравнению с начальными [10]. Выраженность улучшения по сравнению с плацебо в данном исследовании была такой же, как и в работе Beeh и соавт. [21].
Улучшение легочной функции является ключевым моментом в облегчении симптомов ХОЗЛ, особенно одышки. Индексы BDI и TDI позволяют оценивать соответственно одышку, связанную с физической нагрузкой, и изменения выраженности одышки, используя основные факторы, связанные с ее развитием [17]. В масштабных исследованиях было установлено, что у больных среднетяжелым ХОЗЛ тиотропий улучшает оценку TDI по сравнению с плацебо и ипратропием [5-7]. Так как участники настоящего исследования ожидаемо имели лишь незначительную связанную с физической нагрузкой одышку, изменение оценки TDI через 12 нед лечения было маловероятным.
Лечение тиотропием сопровождалось улучшением оценки BDI, хотя различие по сравнению с плацебо не достигло статистической значимости. Кроме того, пациенты, получавшие тиотропий, реже нуждались в использовании сальбутамола по требованию на протяжении всех 12 нед исследования.
Важнейшей задачей при лечении пациентов с ХОЗЛ является улучшение качества жизни, связанного со здоровьем. Большинство участников исследования не имели нарушений по категориям EQ-5D, на которые могло влиять их респираторное заболевание. В то же время значительная часть пациентов отмечали умеренную боль/дискомфорт, а также умеренную тревогу/депрессию. Следовательно, даже легкое ХОЗЛ может вызывать эти нарушения.
В отличие от предыдущих исследований в настоящем исследовании значимых различий между группами тиотропия и плацебо в отношении КЖСЗ не наблюдалось. Это может быть связано с такими факторами. Во-первых, исследование не было спланировано для сравнения различий КЖСЗ между группами. Во-вторых, КЖСЗ оценивали с помощью опросника EQ-5D, а не с использованием инструмента, специально созданного для больных ХОЗЛ, – респираторного опросника Св. Георгия (SGRS) [22]. И, наконец, значение имеет и небольшая продолжительность исследования. Так, ретроспективный анализ исследования с участием больных ХОЗЛ показал, что значимое улучшение по SGRQ (на –6,1 балла по сравнению с начальным) наблюдалось только через 1 год от начала лечения.
Принимая во внимание продолжительность и особенности популяции настоящего исследования, отсутствие значимых изменений одышки и КЖСЗ было ожидаемым. Тем не менее было показано, что поддерживающая терапия тиотропием у пациентов с ХОЗЛ легкой степени обеспечивает реальные преимущества, а именно улучшение легочной функции. В свою очередь, улучшение легочной функции, особенно поддерживаемое на протяжении длительного времени, может помочь пациентам поддерживать более высокий уровень физической активности дольше и в конечном итоге улучшить качество жизни в долгосрочной перспективе.
Таким образом, у пациентов с ХОЗЛ легкой степени согласно шведским критериям (ХОЗЛ легкой степени тяжести по классификации GOLD) 12-недельное лечение тиотропием 18 мкг 1 раз в день улучшает показатели ОФВ1 и ФЖЕЛ по сравнению с плацебо. Полученные результаты позволяют утверждать, что тиотропий обладает высокой эффективностью на всех стадиях ХОЗЛ, в том числе на ранних доклинических стадиях. Для подтверждения клинической значимости этих данных необходимы дальнейшие проспективные исследования.
Литература
1. Rennard S., Decramer M., Calverley P.M.A., et al. Impact of COPD in North America and Europe in 2000: subjects’ perspective of Confronting COPDInternational Survey. Eur Respir J 2002;20:799-805.
2. Lindberg A., Bjerg-Backlund A., Ronmark E., Larsson L.-G., Lundback B. Prevalence and underdiagnosis of COPD by disease severity and the attributable fraction of smoking Report from the Obstructive Lung Disease in Northern Sweden Studies. Respir Med 2006;100:264-72.
3. Rabe K.F., Hurd S., Anzueto A., et al. Global Initiative for Chronic Obstructive Pulmonary Disease. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: GOLD executive summary. Am J Respir Crit Care Med 2007;176:532-55
4. Decramer M., Gosselink R., Rutten-van Molken M., et al. Assessment of progression of COPD: report of a workshop held in Leuven, 11-12 March 2004. Thorax 2005;60:335-42.
5. Vincken W., van Noord J.A., Greefhorst A.P.M., et al. Improved health outcomes in patients with COPD during 1 yr’s treatment with tiotropium. Eur Respir J 2002;19:209-16.
6. Brusasco V., Hodder R., Miravitlles M., Korducki L., Towse L., Kesten S. Health outcomes following treatment for six months with once daily tiotropium compared with twice daily salmeterol in patients with COPD. Thorax 2003;58:399-404.
7. Casaburi R., Mahler D.A., Jones P.W., et al. A long-term evaluation of once-daily inhaled tiotropium in chronic obstructive pulmonary disease. Eur Respir J 2002;19:217-24.
8. Maltais F., Hamilton A., Marciniuk D., et al. Improvements in symptom-limited exercise performance over 8 h with once-daily tiotropium in patients with COPD. Chest 2005;128:1168-78.
9. Niewoehner D.E., Rice K., Cote C., et al. Prevention of exacerbations of chronic obstructive pulmonary disease with tiotropium, a once-daily inhaled anticholinergic bronchodilator: a randomized trial. Ann Intern Med 2005;143:317-26.
10. Adams S.G., Anzueto A., Briggs D.D. Jr., Menjoge S.S., Kesten S. Tiotropium in COPD patients not previously receiving maintenance respiratory medications. Respir Med 2006;100:1495-1503.
11. The Swedish Society of Respiratory Medicine. Nationellt vardprogram for KOL. Available at: www.slmf.se/kol/. Accessed 22 November, 2006.
12. Anon. BTS guidelines for the management of chronic obstructive pulmonary disease. The COPD Guidelines Group of the Standards of Care Committee of the BTS. Thorax 1997;52:1-28.
13. American Thoracic Society. Definitions, epidemiology, pathophysiology, diagnosis, and staging. Am J Respir Crit Care Med 1995;152:S78-S120.
14. Swedish Society for Respiratory Medicine. Nationellt vardprogram for KOL Kroniskt Obstruktiv Lungsjukdom version 1.5 2006. Available at: http://www.slmf.se/kol/.
15. American Thoracic Society. Standardization of spirometry: 1994 update. Am J Respir Crit Care Med 1995;152:1107-36.
16. Quanjer P.H., Tammeling G.J., Cotes J.E., Pedersen O.F., Peslin R., Yernault J.-C. Lung volumes and forced ventilatory flows. Report Working Party Standardization of Lung Function Tests, European Community for Steel and Coal. Official Statement of the European Respiratory Society. Eur Respir J Suppl 1993;16:5-40.
17. Mahler D.A., Weinberg D.H., Wells C.K., Feinstein A.R. The measurement of dyspnea. Contents, interobserver agreement, and physiologic correlates of two new clinical indexes. Chest 1984;85:751-8.
18. Fletcher C.M., Elmes P.C., Fairbain A.S. The significance of respiratory symptoms and diagnosis of chronic bronchitis in working population. BMJ 1959;2:257-66.
19. Anon. EuroQol – a new facility for the measurement of health-related quality of life. The EuroQol Group. Health Policy 1990;16:199-208.
20. Rutten-van Molken M.P., Oostenbrink J.B., Tashkin D.P., Burkhart D., Monz B.U. Does quality of life of COPD patients as measured by the generic EuroQol five dimension questionnaire differentiate between COPD severity stages? Chest 2006;130:1117-28.
21. Beeh K.M., Beier J., Buhl R., Stark-Lorenzen P., Gerken F., Metzdorf N. Efficacy of tiotropium bromide (Spiriva) in patients with chronic-obstructive pulmonary disease (COPD) of different severities. Pneumologie 2006;60:341-6.
22. Jones P.W., Quirk F.H., Baveystock C.M., Littlejohns P. A self-complete measure of health status for chronic airflow limitation. The St. George’s Respiratory Questionnaire. Am Rev Respir Dis 1992;145:1321-7.
Primary Care Respiratory Journal 2008; 17
www.health-ua.com










Комментарии